YC-Startup Felix will Antibiotika durch programmierbare Viren ersetzen
Im Moment befindet sich die Welt im Krieg. Aber das ist kein gewöhnlicher Krieg. Es ist ein Kampf mit einem so kleinen Organismus, dass wir ihn nur mit einem Mikroskop erkennen können – und wenn wir ihn nicht stoppen, könnte er Millionen von uns in den nächsten Jahrzehnten töten. Nein, ich spreche nicht von COVID-19, obwohl dieser Organismus im Moment der in aller Munde ist. Ich spreche von antibiotikaresistenten Bakterien.
Sie sehen, mehr als 700.000 Menschen starben im vergangenen Jahr weltweit an bakteriellen Infektionen – 35.000 davon in den USA. Wenn wir nichts tun, könnte diese Zahl laut einem Bericht der Vereinten Nationen bis 2050 auf 10 Millionen jährlich ansteigen.
Das Problem? Antibiotika-Überbeanspruchung in der Arztpraxis oder in Tier- und Landwirtschaftspraxen. Wir haben im Laufe der Zeit viele Medikamente verwendet, um all die schlechten Bakterien abzutöten – aber es hat nur die meisten, nicht alle, der schlechten Bakterien abgetötet. Und wie die berühmte Zeile von Jeff Goldblum im Jurassic Park sagt, “findet das Leben einen Weg.”
Geben Sie Felix, ein Biotech-Startup in der neuesten Y Combinator-Charge, die glaubt, einen neuartigen Ansatz zu haben, um bakterielle Infektionen in Schach zu halten – Viren.

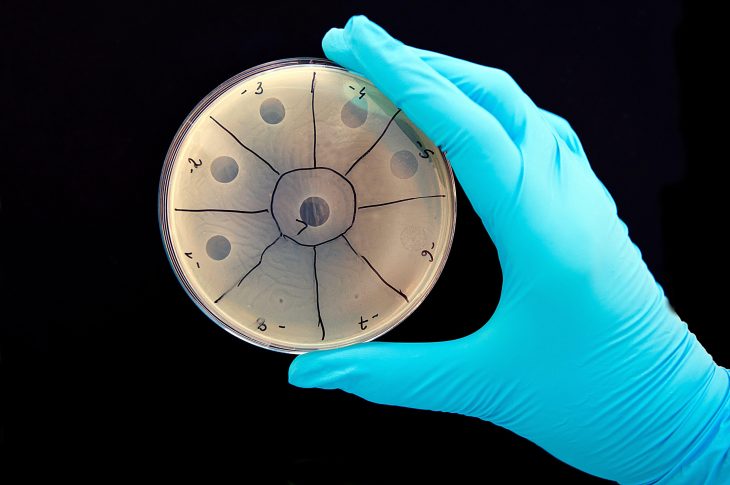
Phage töten Bakterien in einer Petrischale
Es scheint seltsam in einer Zeit der weit verbreiteten Sorge über das Corona-Virus auf jedes Virus in einem guten Licht zu betrachten, aber wie Mitbegründer Robert McBride erklärt, Felix Schlüsseltechnologie ermöglicht es ihm, sein Virus auf bestimmte Standorte auf Bakterien zu zielen. Dies tötet nicht nur die schlechten Bakterien ab, sondern kann auch seine Fähigkeit, sich zu entwickeln und wieder resistent zu werden, aufhalten.
Aber die Idee, ein Virus zu verwenden, um Bakterien abzutöten, ist nicht unbedingt neu. Bakteriophagen oder Viren, die Bakterien “infizieren” können, wurden erstmals 1915 von einem englischen Forscher entdeckt und die kommerzialisierte Phagentherapie begann in den 1940er Jahren in den USA durch Eli Lilly and Company. Gleich dann kamen Antibiotika und westliche Wissenschaftler schienen die Therapie einfach nie weiter zu erforschen.
Da jedoch zu wenige neue Lösungen angeboten werden und das Standard-Drogenmodell nicht effektiv funktioniert, um die Situation zu bekämpfen, glaubt McBride, dass sein Unternehmen die Phagentherapie wieder in den Vordergrund stellen kann.
Felix hat seine Lösung bereits auf einer anfänglichen Gruppe von 10 Personen getestet, um seinen Ansatz zu demonstrieren.
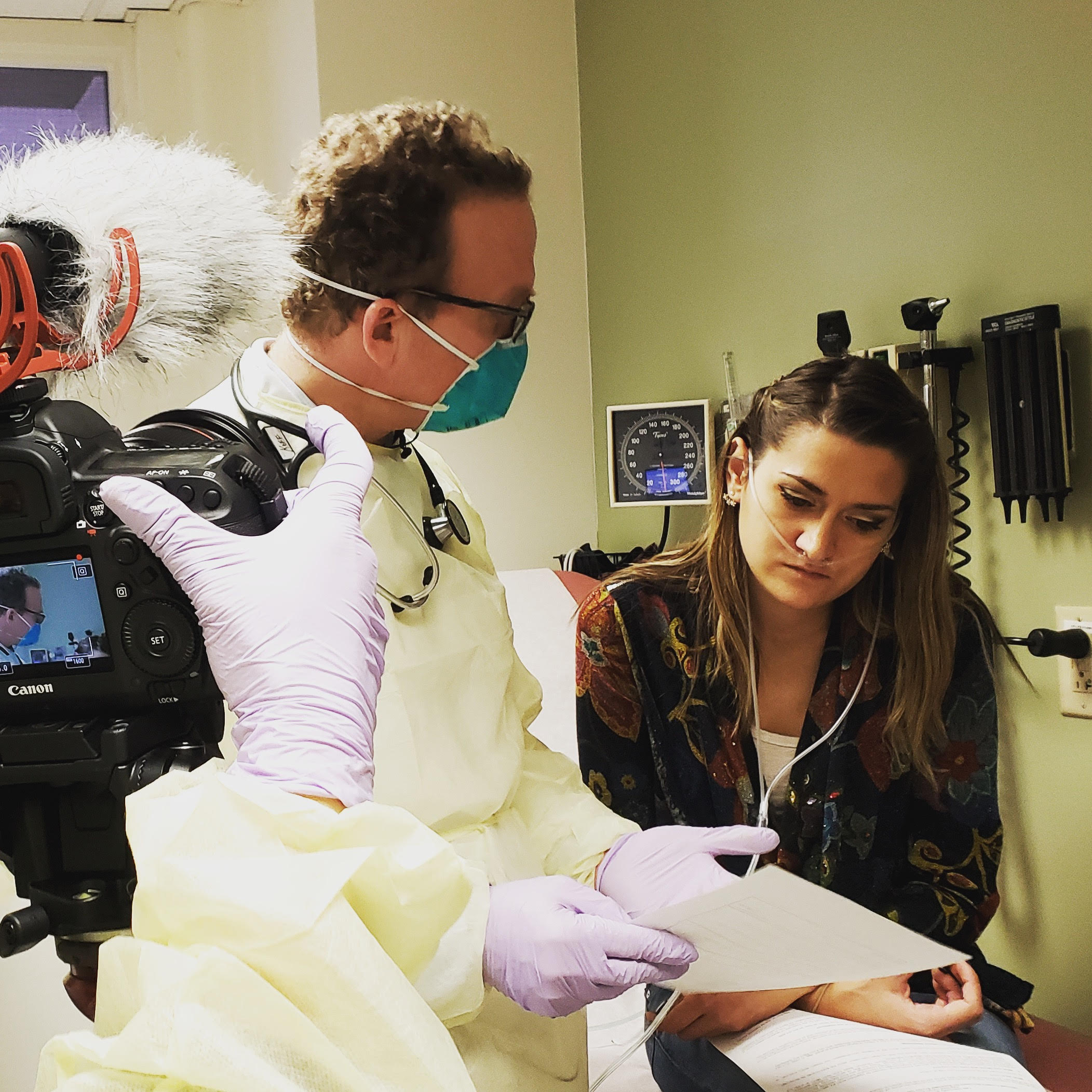
Felix-Forscher hilft Mukoviszidose-Patientin Ella Balasa durch Phagentherapie
“Wir können Therapien in weniger Zeit und für weniger Geld als herkömmliche Antibiotika entwickeln, weil wir auf orphan Indikationen abzielen und wir bereits wissen, dass unsere Therapie beim Menschen funktionieren kann”, sagte McBride gegenüber TechCrunch . “Wir argumentieren, dass unser Ansatz, der Bakterien für traditionelle Antibiotika wieder sensibilisiert, eine First-Line-Therapie sein könnte.”
Felix plant, seine Behandlung für bakterielle Infektionen bei Patienten mit Mukoviszidose zuerst einzusetzen, da diese Patienten dazu neigen, einen nahezu konstanten Strom von Antibiotika zur Bekämpfung von Lungeninfektionen zu benötigen.
Der nächste Schritt wird sein, eine kleine klinische Studie mit 30 Personen durchzuführen, dann, wie das wissenschaftliche Forschungs- und Entwicklungsmodell tendenziell geht, eine größere Studie am Menschen, bevor sie die FDA-Zulassung beantragt. Aber McBride hofft, dass sich seine virale Lösung rechtzeitig bewähren wird, um dem bevorstehenden Ansturm von Antibiotikaresistenzen zu helfen.
“Wir wissen, dass die antibiotikaresistente Herausforderung jetzt groß ist und sich nur noch verschlimmern wird”, sagte McBride. “Wir haben eine elegante technologische Lösung für diese Herausforderung und wir wissen, dass unsere Behandlung funktionieren kann. Wir wollen zu einer Zukunft beitragen, in der diese Infektionen nicht mehr als 10 Millionen Menschen pro Jahr töten, eine Zukunft, auf die wir uns freuen können.”
Keywords: afds, afdsafds










